Prova Transformações Químicas para o Enem | ENEM
📚 Simulado ENEM | Aluno ENEM | cód.14549
Prepare-se com inteligência: resolva o simulado ENEM agora mesmo! 🧠
🎯 São milhares de simulados para concurso disponíveis para você praticar e conseguir a tão sonhada aprovação em Concurso Público.
🧪 Este Simulado ENEM foi elaborado da seguinte forma:
- 📌 Categoria: Enem
- 🏛️ Instituição: ENEM
- 👔 Cargo: Aluno ENEM
- 📚 Matéria: Transformações Químicas
- 🧩 Assuntos do Simulado:
- 🏢 Banca Organizadora: . Bancas Diversas
- ❓ Quantidade de Questões: 10
- ⏱️ Tempo do Simulado: 30 minutos
⚙️ REGRA DO SIMULADO
Este simulado é gratuito 🆓. Basta clicar no botão iniciar abaixo e preencher um breve cadastro para participar do nosso ranking.
📊 No ranking você compara sua nota com outros candidatos e acompanha sua evolução nos estudos.
🚀 Aproveite este simulado ENEM e saia na frente na sua preparação!
📖 Questões ENEM
Se ainda não estiver pronto para fazer o simulado, treine antes com nossas questões de concursos:
🎥 Vídeo Aula
Confira vídeo aulas no YouTube com foco no concurso ENEM. Estude com conteúdo gratuito e atualizado.
Assistir vídeo aula sobre ENEM
📚 Apostila
Encontre apostilas completas e materiais didáticos atualizados para o concurso ENEM.
📢 Concursos Abertos para ENEM
Veja os concursos abertos da instituição ENEM. A lista está sempre atualizada:
🍀 Boa sorte e Bons Estudos,
ConcursosAZ - Aprovando de A a Z ✅
- #188708
- Banca
- . Bancas Diversas
- Matéria
- Transformações Químicas
- Concurso
- ENEM
- Tipo
- Múltipla escolha
- Comentários
- Seja o primeiro a comentar
(1,0) 1 -
No ar que respiramos existem os chamados “gases inertes”. Trazem curiosos nomes gregos, que significam “o Novo”, “o Oculto”, “o Inativo”. E de fato são de tal modo inertes, tão satisfeitos em sua condição, que não interferem em nenhuma reação química, não se combinam com nenhum outro elemento e justamente por esse motivo ficaram sem ser observados durante séculos: só em 1962 um químico, depois de longos e engenhosos esforços, conseguiu forçar “o Estrangeiro” (o xenônio) a combinar-se fugazmente com o flúor ávido e vivaz, e a façanha pareceu tão extraordinária que lhe foi conferido o Prêmio Nobel.
LEVI, P. A tabela periódica. Rio de Janeiro: Relume-Dumará, 1994 (adaptado).
Qual propriedade do flúor justifica sua escolha como reagente para o processo mencionado?
- a) Densidade.
- b) Condutância.
- c) Eletronegatividade.
- d) Estabilidade nuclear.
- e) Temperatura de ebulição.
- #188712
- Banca
- . Bancas Diversas
- Matéria
- Transformações Químicas
- Concurso
- ENEM
- Tipo
- Múltipla escolha
- Comentários
- Seja o primeiro a comentar
(1,0) 2 -
Os bafômetros (etilômetros) indicam a quantidade de álcool, C2H6O (etanol), presente no organismo de uma pessoa através do ar expirado por ela. Esses dispositivos utilizam células a combustível que funcionam de acordo com as reações químicas representadas:

Na reação global de funcionamento do bafômetro, os reagentes e os produtos desse tipo de célula são
- a) o álcool expirado como reagente; água, elétrons e H+ como produtos.
- b) o oxigênio do ar e H+ como reagentes; água e elétrons como produtos.
- c) apenas o oxigênio do ar como reagente; apenas os elétrons como produto.
- d) apenas o álcool expirado como reagente; água, C2H4O e H+ como produtos.
- e) o oxigênio do ar e o álcool expirado como reagentes; água e C2H4O como produtos.
- #188718
- Banca
- . Bancas Diversas
- Matéria
- Transformações Químicas
- Concurso
- ENEM
- Tipo
- Múltipla escolha
- Comentários
- Seja o primeiro a comentar
(1,0) 3 -
A matéria-prima básica para a fabricação de calçados plásticos é a resina de PVC. A seguir é apresentado o fluxograma de fabricação do PVC e sua fórmula química.
Siglas: PVC - policloreto de vinila; EDC - dicloro etano; MVC - monocloreto de vinila

Para a produção do PVC, a obtenção do cloro é proveniente do processo de
- a) destilação.
- b) eletrólise.
- c) fusão ígnea.
- d) filtração a vácuo.
- e) precipitação fracionada.
- #188719
- Banca
- . Bancas Diversas
- Matéria
- Transformações Químicas
- Concurso
- ENEM
- Tipo
- Múltipla escolha
- Comentários
- Seja o primeiro a comentar
(1,0) 4 -
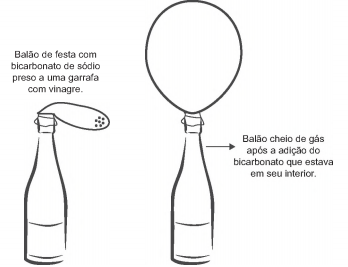
A transformação química em questão é representada pela equação:
- a) CH3COOH (aq) + NaHCO3 (s) → Na+ (aq) + CH3COO- (aq) + CO2 (g) + H2O (l)
- b) CH3COOH (aq) + NaHCO3 (s) → Na+ (aq) + CH3COO- (aq) + O2 (g) + H2O (l)
- c) CH3COOH (aq) + NaHCO3 (s) → Na+ (aq) + CH3COO- (aq) + H2O (l)
- d) CH3COOH (aq) + NaHCO3 (s) → NaCO2+ (aq) + CH3COO- (aq) + H2O (l)
- e) CH3COOH (aq) + NaHCO3 (s) → Na+ (aq) + CH3COO- (aq) + H2 (g) + H2O (l)
- #188721
- Banca
- . Bancas Diversas
- Matéria
- Transformações Químicas
- Concurso
- ENEM
- Tipo
- Múltipla escolha
- Comentários
- Seja o primeiro a comentar
(1,0) 5 -
O mármore é um material empregado para revestimento de pisos e um de seus principais constituintes é o carbonato de cálcio. Na limpeza desses pisos com solução ácida, ocorre efervescência.
Nessa efervescência o gás liberado é o
- a) oxigênio.
- b) hidrogênio
- c) cloro.
- d) dióxido de carbono.
- e) monóxido de carbono.
- #188722
- Banca
- . Bancas Diversas
- Matéria
- Transformações Químicas
- Concurso
- ENEM
- Tipo
- Múltipla escolha
- Comentários
- Seja o primeiro a comentar
(1,0) 6 -
Na mitologia grega, Nióbia era a filha de Tântalo, dois personagens conhecidos pelo sofrimento. O elemento químico de número atômico (Z) igual a 41 tem propriedades químicas e físicas tão parecidas com as do elemento de número atômico 73 que chegaram a ser confundidos. Por isso, em homenagem a esses dois personagens da mitologia grega, foi conferido a esses elementos os nomes de nióbio (Z = 41) e tântalo (Z = 73). Esses dois elementos químicos adquiriram grande importância econômica na metalurgia, na produção de supercondutores e em outras aplicações na indústria de ponta, exatamente pelas propriedades químicas e físicas comuns aos dois.
KEAN, S. A colher que desaparece: e outras histórias reais de loucura, amor e morte a partir dos elementos químicos. Rio de Janeiro: Zahar, 2011 (adaptado).
A importância econômica e tecnológica desses elementos, pela similaridade de suas propriedades químicas e físicas, deve-se a
- a) terem elétrons no subnível f.
- b) serem elementos de transição interna.
- c) pertencerem ao mesmo grupo na tabela periódica.
- d) terem seus elétrons mais externos nos níveis 4 e 5, respectivamente.
- e) estarem localizados na família dos alcalinos terrosos e alcalinos, respectivamente.
- #188723
- Banca
- . Bancas Diversas
- Matéria
- Transformações Químicas
- Concurso
- ENEM
- Tipo
- Múltipla escolha
- Comentários
- Seja o primeiro a comentar
(1,0) 7 -
A Química Verde é um ramo da química que prega o desenvolvimento de processos eficientes, que transformem a maior parte do reagente em produto, de forma mais rápida e seletiva, que utilizem poucos reagentes, que produzam somente o produto desejado, evitando a formação de coprodutos, e que utilizem solventes não agressivos ao meio ambiente. Assim, as indústrias contornariam problemas relacionados à poluição ambiental e ao desperdício de água e energia.
O perfil de um processo que segue todos os princípios desse ramo da química pode ser representado por:
- a) A + B + C → D (a reação ocorre a altas pressões).
- b) A + B → C + D (a reação é fortemente endotérmica).
- c) A + 3B → C (a reação ocorre com uso de solvente orgânico).
- d) 3A + 2B → 2C → 3D + 2E (a reação ocorrre sob pressão atmosférica).
- e) A+1/2B → C (a reação ocorre com o uso de um catalisador contendo um metal não tóxico).
- #188724
- Banca
- . Bancas Diversas
- Matéria
- Transformações Químicas
- Concurso
- ENEM
- Tipo
- Múltipla escolha
- Comentários
- Seja o primeiro a comentar
(1,0) 8 -
As mobilizações para promover um planeta melhor para as futuras gerações são cada vez mais freqüentes. A maior parte dos meios de transporte de massa é atualmente movida pela queima de um combustível fóssil. A título de exemplificação do ônus causado por essa prática, basta saber que um carro produz, em média, cerca de 200 g de dióxido de carbono por km percorrido.
Revista Aquecimento Global. Ano 2, n° 8. Publicação do Instituto Brasileiro de Cultura Ltda.
Um dos principais constituintes da gasolina é o octano (C 8H18). Por meio da combustão do octano é possível a liberação de energia, permitindo que o carro entre em movimento. A equação que representa a reação química desse processo demonstra que
- a) no processo há liberação de oxigênio, sob a forma de O2.
- b) o coeficiente estequiométrico para a água é de 8 para 1 do octano.
- c) no processo há consumo de água, para que haja liberação de energia.
- d) o coeficiente estequiométrico para o oxigênio é de 12,5 para 1 do octano.
- e) o coeficiente estequiométrico para o gás carbônico é de 9 para 1 do octano.
- #188725
- Banca
- . Bancas Diversas
- Matéria
- Transformações Químicas
- Concurso
- ENEM
- Tipo
- Múltipla escolha
- Comentários
- Seja o primeiro a comentar
(1,0) 9 -
Um bafômetro simples consiste em um tubo contendo uma mistura sólida de dicromato de potássio em sílica umedecida com ácido sulfúrico. Nesse teste, a detecção da embriaguez por consumo de álcool se dá visualmente, pois a reação que ocorre é a oxidação do álcool a aldeído e a redução do dicromato (alaranjado) a cromo(lll) (verde) ou cromo(ll) (azul).

A equação balanceada da reação química que representa esse teste é:
- a) Cr2O72- (aq) + 2 H+ (aq) + 3 CH3-CH2-OH (g) → 2 Cr2+ (aq) + 4 H2O (I) + 3 CH3-COOH (g)
- b) Cr2O72- (aq) + 8H+ (aq) + 3 CH3-CH2-OH (g) → 2 Cr3+ (aq) + 7 H2O (I) + 3 CH3-CHO (g)
- c) CrO42- (aq) + 2 H+ (aq) + 3 CH3-CH2-OH (g) → Cr3+ (aq) + 4 H2O (I) + 3 CH3-CHO (g)
- d) Cr2O72- (aq) + 8H+ (aq) + 3 CH3-CHO (g) → 2 Cr3+ (aq) + 4 H2O (I) + 3 CH3-COOH (g)
- e) CrO42- (aq) + 2 H+ (aq) + 3 CH3-CHO (g) → Cr2+ (aq) + H2O (I) + 3 CH3-COOH (g)
- #188726
- Banca
- . Bancas Diversas
- Matéria
- Transformações Químicas
- Concurso
- ENEM
- Tipo
- Múltipla escolha
- Comentários
- Seja o primeiro a comentar
(1,0) 10 -
Os calcários são materiais compostos por carbonato de cálcio, que podem atuar como sorventes do dióxido de enxofre (SO2 ), um importante poluente atmosférico. As reações envolvidas no processo são a ativação do calcário, por meio de calcinação, e a fixação do SO2 com a formação de um sal de cálcio, como ilustrado pelas equações químicas simplificadas.

Considerando-se as reações envolvidas nesse processo de dessulfurização, a fórmula química do sal de cálcio corresponde a
- a) CaSO3 .
- b) CaSO4.
- c) CaS2O8 .
- d) CaSO2 .
- e) CaS2O7 .

